- 网站首页
-
走进协会
- 原料信息
- 金融服务
- 协会资讯
- 政策法规
- 行业资讯
- 相关下载
- 会员中心
详细解读|美国如何监管化妆品用途的OTC产品?相关输美企业如何合规?
发布日期: 2023年10月26日 作者: 瑞欧科技在中国和欧盟,化妆品和药品两类产品的定义有十分清晰的界限。与之不同的是,美国的化妆品和药品却有互相重合的状态,一个产品可以同时是化妆品和非处方类药品(over-the-counter, OTC)。
在美国,哪些化妆品会被划为OTC产品?有哪些监管要求?输美企业应注意哪些合规问题?一起来看:
什么是OTC产品?
在介绍什么是OTC产品前,我们先来分别看美国对于化妆品和药品的定义。
化妆品
根据美国食品药品化妆品法案(FD&C法案),化妆品是指“以涂抹,喷洒或喷涂,或其他途径施用于人体以达到清洁、美化、增进魅力或改善外观为预期目的的物品(肥皂除外)”。
美国的化妆品主要分为彩妆(脸部/眼部,成人/儿童)、烫染发产品、口腔卫生类产品、除臭剂、婴儿产品、个人清洁、美黑产品等17个类别。
药品
药品是指除食品以外,用于诊断、治愈、缓解、治疗或预防疾病的物品以及用于影响人或动物的身体结构或任何功能的物品。
OTC产品
OTC产品是药品的一种,受美国食品药品监督管理局(FDA)的监管。OTC产品必须符合FDA关于产品质量、有效性和安全性的标准。
在美国,OTC产品有很多种,比如常见的止痛药和退烧药、感冒药、止汗剂等都属于OTC产品。
美国目前将部分风险程度较高且含有特定功效活性成分的化妆品归属为OTC产品。这种管理方式往往出现在当化妆品含有2种预期用途且分别符合化妆品和OTC的功效要求时。
举例:去屑洗发水,从清洁头发的功效来看,属于化妆品,从去屑功效来看,属于OTC药品,所以去屑洗发水在美国同时属于化妆品和OTC产品;类似的产品还有含氟化物的牙膏、具有止汗剂的除臭剂以及防晒产品等。
判断产品是否受OTC监管?
那么,如何来确定某个产品在美国是否作为OTC监管呢?一般而言,可以通过以下2种途径:
产品的宣称
包括产品标签、广告和互联网上或其他宣传材料中的宣称。如果化妆品涉及药物功效的宣称,则会被认为需要按照药品监管。
比如,漱口水产品中宣称通过抑制细菌繁殖来缓解口气问题,则会被认为属于药品的功效宣称。
产品的成分
产品中含有的某些被认为是药物的成分或者某成分具有大众熟知或行业认可的治疗用途,如牙膏中的氟化物。
OTC专论
这里还有一个比较实操的方式,就是参考美国的OTC专论(OTC Monograph),这些专论可以看成是具有特定药物功效的活性成分的标准。
如果一种成分记载在专论中,且成分功效与产品功效宣称相符,大概率所属产品会被作为OTC管理。
OTC专论中与化妆品相关的活性成分功效主要包括:祛痘/痤疮治疗的成分、防晒成分、防龋成分、牙齿脱敏成分、某些皮肤保护剂(如收敛剂、治疗皮肤干燥或开裂、尿布疹治疗相关成分等)、去屑成分、抗菌成分、止汗剂相关的成分,等等。 美国对OTC产品的监管要求
符合OTC专论
在OTC专论中的活性成分通常被认为是安全有效的(Generally Recognized as Safe and Effective, GRASE),即如果一种活性成分在FDA的OTC专论中,在符合专论相关要求的前提下,意味着FDA已经确认了它在产品中的安全性和有效性。
专论中会提供活性成分的使用要求和限制、标签和其他的一般要求。如果产品符合专论中的要求,则产品上市前可以进行简单的产品列名,不需要经过FDA的批准。
新药申请
如果不符合OTC专论,那么产品的合规路径是进行新药申请(New drug application),通过这个途径申请需要递交完整的药物申请资料,想必化妆品企业是不会考虑该方案的。
活性成分在OTC专论中的产品,虽然无需经过FDA的上市前审批,但仍然需要满足其他的合规要求:
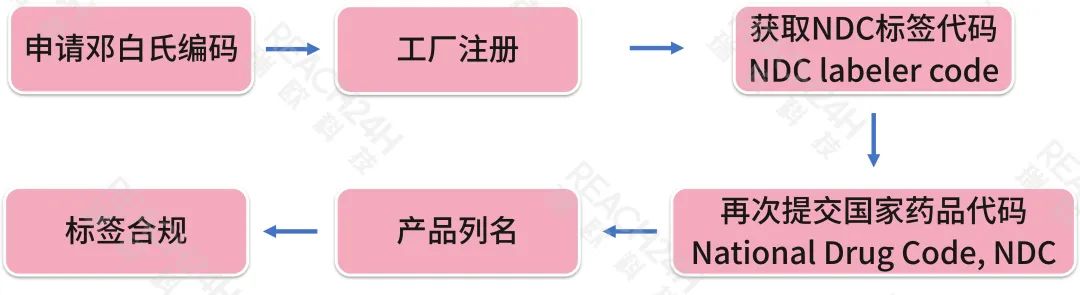
OTC专论药物的注册流程
如OTC相关的工厂必须进行工厂注册,也需要遵守FDA相关的GMP;上市销售的OTC产品必须取得国家药品代码(NDC)(用于标识药品及其包装的11位数字识别码);OTC产品在产品上市销售5天内完成产品列名;并且需要遵守OTC产品相关的标签要求。
需要注意的是,在美国化妆品法规现代化法案(MoCRA)实施以后,化妆品也需要进行相关的工厂注册和产品列名,该工厂注册和产品列名与OTC的工厂注册和产品列名并不在同一个平台。
另外,如果产品既属于化妆品又属于OTC,无需再进行化妆品平台的产品列名。
相关阅读友情链接政府网站中国政府网 国家药品监督管理局 国家市场监督管理总局 国家知识产权局 国家商务部 国家卫生健康委员会 国家海关总署 国家工业和信息化部 国家科学技术部 国家发展和改革委员会 国家统计局 省药品监督管理局 省市场监督管理局(知识产权局) 省卫生健康委员会 省工业和信息化厅 省科学技术厅 汕头市政府网 市市场监督管理局(知识产权局) 市工业和信息化局 市科学技术局 市商务局(口岸局) 市贸易促进委员会 市工商业联合会(总商会)相关网站版权所有 | 汕头市化妆品行业协会TEL:0754-88658188 | FAX:0754-88658122QQ:773788949 | E-mail:773788949@qq.com地址:汕头市龙湖区电信实业大厦1609室 | 邮编:515000备案号:粤ICP备20001656号
 @鑫煌科技@鑫嵘科技技术支持
@鑫煌科技@鑫嵘科技技术支持
- 原料信息
